Bolile inflamatorii intestinale (BII) sunt afecțiuni cronice, incurabile și dizabilitante cu o incidență în continuă creștere. Ele afectează în special populația activă și, prin urmare, o identificare precoce a lor are un impact major în evoluția lor. Această lucrare își propune să găsească o modalitate simplă de diagnostic precoce a bolilor inflamatorii intestinale (BII) în asistența medicală primară.
Abstract
Inflammatory bowel diseases (IBD) are chronic, incurable and disabling conditions with increasing incidence. They especially affect the active population and an early identification has a major impact for evolution of those diseases. This work aims to find a simple way of early diagnosis in primary care for inflammatory bowel diseases (IBD).
Bolile inflamatorii intestinale (BII) sunt afecțiuni cronice, incurabile și invalidante, cu o incidență în continuă creștere. S-a constatat o creștere cu 71% a incidenței acestor boli din anul 2000 până în 2019. Această incidență este în continuă creștere. Prevalența cea mai crescută se remarcă la populația activă (grupa de vârstă 50-59 de ani), la ambele sexe.
Țările nordice înregistrează cele mai înalte rate de prevalență, Norvegia ocupând primul loc (Fig. 1).

Fig. 1. Incidența și prevalența bolilor inflamatorii intestinate la nivel european
Bolile inflamatorii intestinale (BII) sunt reprezentate de două entități: rectocolita ulcero-hemoragică (RCUH) și boala Crohn (BC).
Rectocolita ulcero-hemoragică (RCUH) reprezintă o afecțiune inflamatorie limitată la nivelul colonului și rectului pe când boala Crohn (BC) este o inflamație regăsită și în alte regiuni ale tractului gastro-intestinal (de la zona perianală până la cavitatea bucală).
Cauzele acestor afecțiuni nu sunt stabilite cu exactitate, dar se pare că ele ar fi consecința unei interacțiuni complexe între predispoziția genetică, mediu (microbiomul intestinal) și sistemul imunitar ale persoanei afectate.
Sunt boli cu mecanism încă neelucidat, mecanismele fizio-patologice cele mai probabile fiind cele autoimune sau infecțioase.
Au evoluție fluctuantă, cu pusee active și perioade de remisiune.
În timp ce rectocolita ulcero-hemoragică (RCUH) este limitată la mucoasa colonică, boala Crohn (BC) afectează transmural peretele intestinal (Fig. 2).

Fig. 2. Bolile inflamatorii intestinale
Referitor la leziunile perianale ale bolii Crohn se contată la nivel european o prevalență crescută în țările nordice (Norvegia, Suedia, Danemarca), dar și în Olanda, Germania. De asemenea este de remarcat o prevalență crescută în Ungaria.
În România se înregistrează o prevalență scăzută comparativ cu restul Europei.
De subliniat că nu se cunosc date exacte ale prevalenței acestor boli în multe țări europene atât din estul dar și din vestul Europei (ex: Franța) (fig 3).

Plecând de la aceste date, putem afirma că bolile inflamatorii intestinale constituie o categorie de afecțiuni care nu fac parte din practica zilnică a medicilor în general și implicit a medicilor de familie.
Fiecare medic de familie îngrijește maxim 10 pacienți cu boli inflamatorii intestinale.
De cele mai multe ori pacienții sunt diagnosticați după o perioadă îndelungată de la debutul simptomatologiei și frecvent ca urmare a instalării complicațiilor bolii.
Drumul unui astfel de pacient cunoaște numeroase trasee în sistemul medical, iar diagnosticul este stabilit frecvent în stadii avansate de boală.
Confruntându-ne cu cazuri complicate de boli inflamatorii intestinale, ne-am ridicat problema dacă putem scurta drumul de la debutul bolii până la stabilirea diagnosticul unui astfel de pacient.
Există elemente cheie pentru un diagnostic precoce al pacientului cu boală inflamatorie intestinală în medicina primară?
În acest sens Grupul GastRo al SNMF împreună cu Clubul Român pentru Boala
Crohn și Colită Ulcerativă și Societatea Română de Gastroenterologie și Hepatologie din România au elaborat o scrisoare metodologică privind diagnosticul și tratamentul pacienților cu boli inflamatorii intestinale.
Scopul acestei scrisori este de a ajuta medicii de familie să identifice mai ușor și mai rapid un pacient cu boală inflamatorie intestinală. Odată identificat, acest pacient este recomandat să aibă un traseu bine stabilit și să fie trimis pentru confirmarea diagnosticului într-un centru integrat, cu expertiză în abordarea acestor patologii.
Monitorizarea și managementul corect al unui astfel de pacient, într-o echipă multidisciplinară, contribuie la supravegherea atentă și la identificarea rapidă a puseelor active de boală precum și la intervenții rapide și eficiente.
Principalele simptome cu care se prezintă un pacient cu boală inflamatorie intestinală (BII) la medicul de familie sunt:
- Diaree cronică
- Durere abdominală
- Fatigabilitate
- Scădere ponderală
Diareea cronică și durerea abdominală reprezintă simptome comune ale bolilor inflamatorii intestinale (BII) dar și ale altor tulburări funcționale digestive și de aceea diagnosticul diferențial este extrem de important.
Diareea cronică mai ales diareea sangvinolentă este frecventă în rectocolita ulcero-hemoragică, pe când pacientul cu boală Crohn are de obicei ca simptom central durerea abdominală cronică.
Fatigabilitatea și scăderea ponderală sunt consecința malnutriției și a malabsorbției din aceste boli.
Malnutriția se instalează prin faptul că pacientul își reduce aportul alimentar, deoarece constată că simptomatologia se agravează postprandrial.
Malabsorbția apare prin scăderea absorbției intestinale consecința leziunilor inflamatorii de la acest nivel.
Plecând de la aceste simptome, scrisoarea metodologică propune medicului de familie utilizarea unui algoritm de identificare rapidă a pacientului cu posibilă boală inflamatorie intestinală (BII).
Acest algoritm cuprinde trei pași pentru pacientul cu simptome sugestive de boală inflamatorie intestinală (BII) (Fig.4)
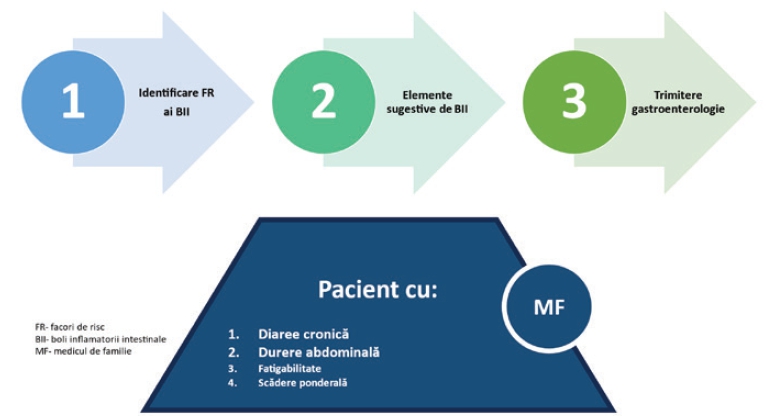
- Identificarea activă a factorilor de risc de boli inflamatorii intestinale (BII)
- Identificarea activă a elementelor cheie sugestive de boli inflamatorii intestinale (BII)
- Trimiterea țintită într-un centru dedicat bolilor inflamatorii intestinale (BII)
Asftel încât oricărui pacient cu diaree cronică, durere abdominală, fatigabilitate sau scădere ponderală, merită să i se identifice activ factorii de risc de boli inflamatorii intestinale (BII)
Factorii de risc pentru apariția bolilor inflamatorii intestinale (BII) sunt reprezentați de:
- fumat (risc pentru BC)
- istoric de gastro-enterocolite infecțioase
- uz îndelungat de antibiotice sau antiinflamatoare nesteroidiene
- consum de alimente intens procesate, exces de glucide, proteine, deficit de fibre
- stres psiho-emoțional, depresie
Acești factori de risc sunt frecvent identificați în societatea actuală, mai ales în mediul urban și ar putea reprezenta explicația exploziei bolilor inflamatorii intestinale din ultimile două decade (Fig.5).

Fig. 5 Factorii de risc ai bolilor inflamatorii intestinale (BII)
Cu siguranță că la majoritatea pacienților cu simptome sugestive de boli inflamatorii intestinale (BII) vor fi identificați și factori de risc (FR) și de aceea esențial este pasul doi al algoritmului de identificare rapidă a pacientului cu boli inflamatorii intestinale (BII) și anume depistarea activă a elementelor cheie înalt sugestive de boală inflamatorie intestinală (BII).
Acestea sunt reprezentate de:
- diaree nocturnă
- prezența de produse patologice în scaun (sânge, mucus, puroi)
- scădere ponderală > 5%
- afectare perianală cronică (fisuri, fistule, abcese recidivante)
- asocierea manifestărilor extraintestinale (articulare, oculare, cutanate)
- rude de gradul I cu boli inflamatorii intestinale (BII)
- sindrom inflamator asociat tulburărilor de tranzit sau durerii abdominale:
- markeri serologici: PCR, VSH, fibrinogen
- markeri fecali: calprotectina fecală
Diagnosticul și tratamentul BII presupun o abordare integrată și multidisciplinară care să cuprindă o rețea locală, regională, națională de medici specialiști non-gastroenterologi instruiți cu privire la manifestările bolilor inflamatorii intestinale (BII) care să asigure o abordare diagnostică și terapeutică integrată și multidisciplinară.
Echipa de îngrijire a pacientului cu boală inflamatorie intestinală (BII) are nevoie de specialiști dedicați și cu expertiză înaltă în această patologie (Fig.6).
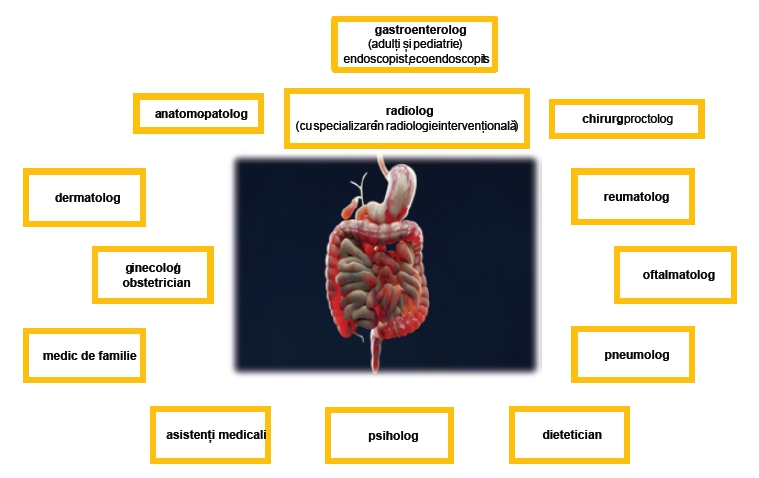
Fig. 6 Echipa de îngrijire a pacientului cu boală inflamatorie intestinală (BII)
Pacienții cu diagnostic confirmat de boală inflamatorie intestinală (BII) necesită monitorizare periodică (medic de familie, gastroenterolog) în vederea urmăririi respectării indicațiilor dietetice și a statusului nutrițional.
Complianța pacienților cu boală Crohn la recomandarea de oprire a fumatului reprezintă o necesitate. Urmărirea respectării terapiei indicate precum și supravegherea reacțiilor adverse asociate tratamentului sunt alte elemente esențiale monitorizării la medicul de familie a unui pacient cu boală inflamatorie intestinală (BII).
Reacțiile adverse asociate tratamentului bolilor inflamatorii intestinale (BII) sunt multiple și recunoașterea timpurie influențează evoluția bolii.
La glucocorticoizi reacțiile adverse cele mai frecvente sunt reprezentate de: retenția sodată, diabetul zaharat, hipertensiunea arterială, glaucomul, depresia, anxietatea, psihozele.
De asemenea pacienții cu boală inflamatorie intestinală (BII) în tratament cu glucocorticoizi pot suferi necroză aseptică de cap femoral sau insuficiență corticosuprarenală la oprirea corticoterapiei.
La pacienții cu boli inflamatorii intestinale (BII) în tratament cu azatioprina este esențială monitorizarea lipazei și amilazei.
Dacă pacientul cu boală inflmatorie intestinală (BII) urmează un tratament anti-TNF alfa este necesar ca acesta să fie evaluat asupra statusului TBC înainte de inițiere. Va evita expunerea la soare sau vaccinarea cu vaccinuri vii (BCG, ROR, anti-varicelos, anti-rotavirus, anti-febră galbenă samd).
Monitorizarea strictă și recunoașterea semnelor de detecție incipientă a puseelor de activitate ale bolii precum și ale complicațiilor (stenoze, abcese, fistule, suprainfecții cu Clostridium Difficile, Cytomegalovirus/CMV, etc) sunt alte obiective ale monitorizării eficiente la medicul de familie a unui astfel de pacient.
Pacientul are nevoie să cunoască în detaliu toate fațetele acestor maladii, să știe când să se alarmeze și unde să apeleze.
Cu siguranță este un pacient fragil iar medicul curant are un loc definitoriu în viața lui.
Informații pertinente, avizate precum și susținere, pacientul cu boală inflamatorie intestinală le poate regăsi și în cadrul ASPIIR (Asociația Persoanelor cu Boli Inflamatorii Intestinale și Stome din România).
Pentru pacientul cu boală inflamatorie intestinală există entități medicale (grupul de lucru GastRO al SNMF care asigură legătura cu medicii de familie din România, Clubul Român pentru Boala Crohn și Colită Ulcerativă și Societatea Română de Gastroenterologie și Hepatologie din România care asigură expertiza și susținerea din cadrul rețelelor sanitare- secundară și terțiară) dar și nemedicale (Asociația Persoanelor cu Boli Inflamatorii Intestinale și Stome din România).
Ele asigură un mediu colaborativ pentru abordarea eficientă a pacientului cu boală inflamatorie intestinală (Fig. 7).
Recunoașterea factorilor de risc dar mai ales a elementelor cheie înalt sugestive de boli inflamatorii intestinale (BII) de către majoritatea medicilor de familie alături de direcționarea acestor pacienți în cadrul unor centre dedicate unde este posibilă abordarea integrată și complexă a acestora, cu siguranță ar contribui la reducerea formelor severe de boală și la îmbunătățirea calității vieții pacienților cu aceste suferințe.
Bibliografie:
- Foto Shutterstock
- Foto UEG Image Hub
- From symptom to diagnosis: clinical distinctions among various forms of intestinal inflammation. Sands BE Gastroenterology. 2004;126(6):1518.
- https://www.gastromf.ro/scrisoare-metodologica-privind-diagnosticul-si-tratamentul-pacientilor-cu-boli-inflamatorii-intestinale
- Toward an integrated clinical, molecular and serological classification of inflammatory bowel disease: report of a Working Party of the 2005 Montreal World Congress of Gastroenterology. Silverberg MS, Satsangi J, Ahmad T, Arnott ID, Bernstein CN, Brant SR, Caprilli R, Colombel JF, Gasche C, Geboes K, Jewell DP, Karban A, Loftus EV Jr, Peña AS, Riddell RH, Sachar DB, Schreiber S, Steinhart AH, Targan SR, Vermeire S, Warren BF SO Can J Gastroenterol. 2005;19 Suppl A:5A.
- The Montreal classification of inflammatory bowel disease: controversies, consensus, and implications.Satsangi J, Silverberg MS, Vermeire S, Colombel JF Gut. 2006;55(6):749.
- Crohn’s disease. Baumgart DC, Sandborn WJ Lancet. 2012;380(9853):1590. Epub 2012 Aug 20.
- Association analyses identify 38 susceptibility loci for inflammatory bowel disease and highlight shared genetic risk across populations.Liu JZ, van Sommeren S, Huang H, Ng SC, Alberts R, Takahashi A, Ripke S, Lee JC, Jostins L, Shah T, Abedian S, Cheon JH, Cho J, Daryani NE, Franke L, Fuyuno Y, Hart A, Juyal RC, Juyal G, Kim WH, Morris AP, Poustchi H, Newman WG, Midha V, Orchard TR, Vahedi H, Sood A, Sung JJ, Malekzadeh R, Westra HJ, Yamazaki K, Yang SK, International Multiple Sclerosis Genetics Consortium, International IBD Genetics Consortium, Barrett JC, Franke A, Alizadeh BZ, Parkes M, B K T, Daly MJ, Kubo M, Anderson CA, Weersma RK, IBD Genetics Consortium Nat Genet. 2015 Sep;47(9):979-86. Epub 2015 Jul 20.
- ACG Clinical Guideline: Ulcerative Colitis in Adults.Rubin DT, Ananthakrishnan AN, Siegel CA, Sauer BG, Long MD Am J Gastroenterol. 2019;114(3):384.
- WSES-AAST guidelines: management of inflammatory bowel disease in the emergency setting Belinda De Simone1* , Justin Davies2 , Elie Chouillard1 , Salomone Di Saverio3 , Frank Hoentjen4 , Antonio Tarasconi5 , Massimo Sartelli6 , Walter L. Biffl7 , Luca Ansaloni8 , Federico Coccolini9 , Massimo Chiarugi9 , Nicola De’Angelis10, Ernest E. Moore11, Yoram Kluger12, Fikri Abu-Zidan13, Boris Sakakushev14, Raul Coimbra15, Valerio Celentano16, Imtiaz Wani17, Tadeja Pintar18, Gabriele Sganga19, Isidoro Di Carlo20, Dario Tartaglia21, Manos Pikoulis22, Maurizio Cardi23, Marc A. De Moya24, Ari Leppaniemi25, Andrew Kirkpatrick26, Vanni Agnoletti27, Gilberto Poggioli28, Paolo Carcoforo29, Gian Luca Baiocchi30 and Fausto Catena5 De Simone et al. World Journal of Emergency Surgery (2021)
- https://www.cghjournal.org/article/S1542-3565(20)30185-3/fulltext
- World Gastroenterology Organisation Global Guidelines Inflammatory Bowel Disease Update August 2015 Review team Charles Bernstein Canada (Chair) Abraham Eliakim Israel Suleiman Fedail Sudan Michael Fried Switzerland Richard Gearry New Zealand Khean-Lee Goh Malaysia Saeed Hamid Pakistan Aamir Ghafor Khan Pakistan Igor Khalif Russia Siew C. Ng Hong Kong, China Qin Ouyang China Jean-Francois Rey France Ajit Sood India Flavio Steinwurz Brazil Gillian Watermeyer South Africa Anton LeMair The Netherland
- ECCO Guideline/Consensus Paper ECCO Guidelines on the Prevention, Diagnosis, and Management of Infections in Inflammatory Bowel Disease T. Kucharzik,a P. Ellul,b T. Greuter,c J. F. Rahier,d B. Verstockt,e, C. Abreu,f A. Albuquerque,g M. Allocca,h M. Esteve,i F. A. Farraye,j H. Gordon,k K. Karmiris,l U. Kopylov,m J. Kirchgesner,n E. MacMahon,o F. Magro,p, C. Maaser,q L. de Ridder,r C. Taxonera,s, M. Toruner,t L. Tremblay,u M. Scharl,v N. Viget,w Y. Zabana,i S. Vavrickav; on behalf of the European Crohn’s and Colitis Organisation [ECCO) Journal of Crohn’s and Colitis, 2021, 879–913 doi:10.1093/ecco-jcc/jjab052 Advance Access publication March 17, 2021 ECCO Guideline/Consensus Paper
 Dr. Mihaela Udrescu
Dr. Mihaela Udrescu











