Degenerescența maculară legată de vârstă (DMLV) este o boală degenerativă ce începe cu acumularea de druseni, modificări pigmentare, cu progresie graduală spre atrofie de EPR. La unii ochi se dezvoltă neovascularizație coroidiană dar substratul fiziopatologic inițial este comun și pentru forma uscată și pentru cea exudativă a DMLV.
Prevalența globală: De la 196 milioane persoane afectate în 2020, se estimează o creștere la 288 milioane de persoane afectate de DMLV până în 2040, pe măsura îmbătrânirii populației planetei.
Pentru a estima riscul de progresie spre forma avansată a bolii, analizăm următoarele elemente: drusen mare (soft) ≥ 125 µm, modificări pigmentare/hiperpigmentări focale (depozite pigmentare, punctiforme, liniare sau reticulare). Recomandăm administrarea de suplimente cu vitamine și antioxidanți (formula din studiul AREDS 2), oprirea fumatului, modificarea dietei cu includerea legumelor verzi, fructelor și peștelui bogat în acizi grași, autotestarea săptămânală cu grila Amsler și prezentare rapidă în cazul de apariție a metamorfopsiilor (deformări ale liniilor drepte). Pacienții cu DMLV neovasculară la un ochi sunt sfătuiți să urmărească foarte atent vederea la celălalt ochi și să se prezinte rapid la consult când sesizează modificări.
Modalități imagistice de evaluare a DMLV atrofică
Alături de fotografia color a fundului de ochi, autofluorescența în lumina albastră sau near-infrared este cea mai bună modalitate de a evalua progresia atrofiei geografice. Lipofuscina din celulele EPR este sursa fluorescenței: pierderea celulelor EPR se evidențiază ca hipofluorescență concomitent cu hiperfluorescența celulelor EPR în suferință de la marginea leziunilor ce pot avea pattern-uri diferite, cele asociate cu un mai mare risc de progresie fiind pattern-ul difuz; pentru evidențierea implicării foveei, tehnica near-infrared permite determinarea aspectului de ,,foveal sparing” ce explică AV încă bună a pacientului.
OCT-ul combinat cu analiza imaginilor folosind inteligența artificială reprezintă standardul de aur în diagnosticul și monitorizarea progresiei leziunilor.
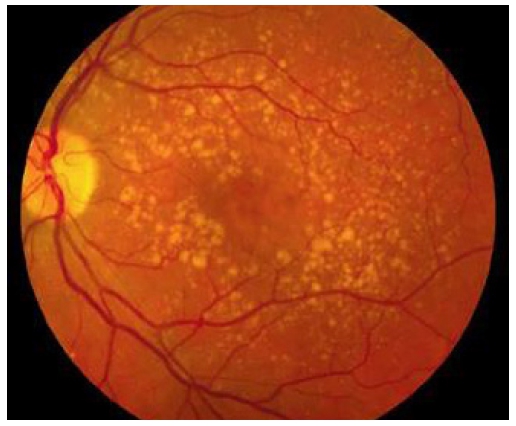
Pentru formele mixte (atrofie geografică combinată cu neovascularizație coroidiană), angiografia-OCT poate înlocui angiografia cu fluoresceină.
Conform consensului terminologiei actuale, în clasificarea CAM (Classification of Atrophy Meeting) bazată pe aspectul OCT, atrofia geografică (cRORA) constă în: zonă de hipertransmisie în coroidă cu diametrul ≥ 250 µm, atrofia EPR și pierderea fotoreceptorilor, în absența semnelor de ruptură a EPR.
O schimbare de paradigmă în DMLV atrofică: tratamentul prin injecții intravitreene
Intrăm într-o nouă eră pentru DMLV atrofică, de la o afecțiune netratabilă spre o afecțiune cronică în care vom administra tratament prin injecții intravitreene. Studiile recente au arătat că în patofiziologia DMLV atrofică este implicată calea complementului. 2 agenți terapeutici au dovedit rezultate pozitive în studiile de fază 3 în atrofia geografică: pegcetacoplan (inhibitor C3)și avacincaptad pegol (inhibitor C5).
Scopul tratamentului este oprirea extinderii ariilor de atrofie, încetinirea progresiei spre fovee și menținerea vederii. Deoarece celulele receptoare pierdute nu pot fi înlocuite, tratamentul aplicat cât mai precoce ar putea salva vederea utilă a pacienților.
Factorii de risc în progresia atrofiei geografice sunt: mărimea leziunii (leziunile mari cresc mai rapid), focalitatea (leziunile multifocale progresează mai rapid), localizarea (leziunile extrafoveale progresează mai repede), pattern-ul la autofluorescență (leziunile difuze au risc mai mare de progresie).
Selecția pacienților care ar putea beneficia cel mai mult de tratament este foarte importantă. Necesită tratament imediat pacienții care prezintă factorii de risc enumerați mai sus, dar au șanse mai mari să beneficieze de tratament pacienții cu leziuni extrafoveale și cu o vedere utilă la baseline ≥ 60 litere ETDRS.
Studiile OAKS și DERBY au evaluat eficacitatea și siguranța tratamentului cu pegcetacoplan (inhibitor al complementului C3) administrat în injecții intravitreene lunare sau la 2 luni (EOM). Studiul OAKS arată o reducere cu 75% a pierderii fotoreceptorilor prin inhibarea complementului, iar în studiul DERBY o reducere de 77% a pierderii de fotoreceptori. Efectul advers cel mai important a fost neovascularizația coroidiană.
În februarie 2023, FDA a aprobat medicamentul pegcetacoplan 15mg / 0.1 ml (SYFOVRE) produs de firma Apellis ca primul tratament injectabil pentru pacienții cu atrofie geografică.
Noi agenți terapeutici cu ținte combinate în tratamentul DMLV neovasculară
Obiectivele actuale în tratamentul DMLV sunt îmbunătățirea acuității vizuale (AV) și reducerea frecvenței injectărilor prin noi agenți terapeutici care să îmbunătățească eficacitatea tratamentului, concomitent cu creșterea duratei de acțiune.
În condiții patologice, angiopoetina 2 blochează angiopoetina 1 de la activarea receptorului TIE2, declanșând o cascadă de evenimente ce conduc la instabilitate vasculară manifestată prin leakage, inflamație și neovascularizație. Creșterea eficienței tratamentului se obține combinând agenți cu mecanisme de acțiune diferite prin inhibarea atât a angiopoetinei 2, cât și a VEGF-A (Aflibercept + Nesvacumab) sau utilizând un singur agent terapeutic ce acționează pe cele 2 mecanisme simultan cum este Faricimab (anticorp bispecific).
În studiile TENAYA și LUCERNE, pacienții cu neovascularizație coroidiană subfoveală sau juxtafoveală au primit în primul an Aflibercept 2mg/8 săptămâni sau Faricimab 6mg la 8, 12 și 16 săptămâni. În anul 2, în regimul PTI (personalized treatment interval), intervalul de administrare a crescut cu 4 săptămâni, cu monitorizarea AV, grosimii foveale centrale sau prezenței hemoragiilor maculare.
AV la pacienții tratați cu faricimab nu a fost inferioară celor tratați cu Aflibercept după 1 an și s-a menținut și la 2 ani, cu intervale de administrare mergând până la 16 săptămâni.
Efectul de creștere a durabilității tratamentului cu Faricimab a fost dovedit în studiile TENAYA și LUCERNE prin faptul că peste 60% dintre pacienți au putut fi tratați la intervale de 16 săptămâni în 2 ani de urmărire.
În privința siguranței și tolerabilității, studiile TENAYA ȘI LUCERNE au arătat un profil similar între Aflibercept și Faricimab, privind efectele adverse oculare de tip inflamator și nu s-a înregistrat niciun caz de vasculită ocluzivă retiniană.
Implicațiile pentru practica clinică: pacienții care nu răspund bine la terapia antiVEGF anterioară, menținând lichid intra/subretinian sunt candidații potriviți pentru tratamentul cu faricimab.
Studiul TRUCKEE, observațional, independent, cuprinde 465 pacienți cu DMLV din care 8,4% netratrați anterior și 91,4% tratați cu agenți antiVEGF (majoritar cu Aflibercept) care au primit Faricimab intravitrean. Studiul prezentat la EURORETINA 2022 a evidențiat rezultate favorabile pentru Faricimab în privința reducerii grosimii centrale foveale și resorbției fluidului intra/subretinian.
În ianuarie 2023, Faricimab (Vabysmo/Genetech) a primit aprobarea FDA pentru tratament în DMLV neovasculară și edemul macular diabetic.
Noi abordări în DMLV forma neovasculară
În DMLV, introducerea terapiei antiVEGF a reprezentat un mare pas înainte. Dar din cauza frecvenței injecțiilor/controalelor de monitorizare, mulți pacienți sunt încă insuficient tratați, ceea ce face ca AV să fie inferioară nivelului obținut în studiile clinice. Noile abordări tehnologice sunt: implantul antiVEGF și terapia genică (înțeleasă ca o biofabrică ce produce un agent antiVEGF). Limitările actuale sunt legate de profilul de siguranță, evidențiindu-se în unele cazuri atrofii de EPR, modificări pigmentare, inflamații și hipotonie oculară.
Terapia genică pentru DMLV: 2 studii clinice de fază 3, ATMOSPHERE și ASCENT investighează terapia genică prin agentul RG X 314 ce codifică producerea unui fragment de anticorp monoclonal similar cu Ranibizumab în celulele retinene. Calea de administrare este subretiniană în intervenția chirurgicală de vitrectomie. S-au obținut nivele înalte de ranibizumab intraocular, asigurând o vedere stabilă, reducerea necesității de reinjectări ulterioare și efect durabil al tratamentului, fără administrare de steroizi profilactic.
Studiul OPTIC de fază 1 evaluează siguranța administrării intravitreene a terapiei genice cu ADVM-022 (ce codifică producerea în celulele retiniene a unei proteine similară cu Aflibercept) și evidențiază că necesitatea de suplimentare cu aflibercept s-a redus cu 68%, concomitent cu menținerea unei AV stabile pe termen lung și atingerea criteriilor de siguranță.
O nouă și promițătoare tehnologie este administrarea unui agent antiVEGF prin intermediul unui implant numit PDS (port delivery system), poziționat chirurgical, ce eliberează constant ranibizumab în cavitatea vitreană și se reumple la fiecare 6 luni (aprobat FDA în 2021).
Studiul ARCHWAY faza 3 compară PDS cu ranibizumab 100mg/l cu reumplere la 24 de săptămâni cu administrarea intravitreană de ranibizumab 0,5 mg la 4 săptămâni. 93% din pacienți cu PDS preferă acest sistem față de injecțiile intravitreene. La OCT se evidențiază rezultate comparabile privind absența fluidiului subretinian/intraretinian, stabilizarea afecțiunii și AV mai bună. Selecția pacienților este esențială pentru obținerea unor rezultate bune ale PDS, iar tehnica chirurgicală este esențială pentru evitarea și minimizarea complicațiilor.
Concluzii
Introducerea injecțiilor intravitreene cu Syfovre (pegcetacoplan) în schema de tratament pentru prevenirea atrofiei geografice reprezintă cel mai important eveniment în oftalmologia ultimilor 10 ani.
În DMLV neovasculară, creșterea duratei de acțiune și a eficacității tratamentului cu ținte combinate/terapie genică/implante cu antiVEGF contribuie la reducerea frecvenței injectărilor cu beneficii atât pentru pacienți, cât și pentru medici.
Toate aceste noi abordări terapeutice revoluționare aduc o nouă speranță pacienților afectați de DMLV.

 Dr. Cristina David
Dr. Cristina David








